长筒花叶片离体培养体系优化 | 灭菌方法与激素配比关键技术
摘要:为建立长筒花的叶片离体培养体系,以苦苣苔科长筒花属长筒花品种‘kimblue’的叶片作为外植体,探索培养过程中各个可能影响培养结果的因素,包括灭菌时长的不同组合、灭菌方法,各培养阶段的激素种类及其配比,进而筛选出影响因素的最佳值。结果显示,叶片外植体最适的灭菌组合和方法为75%酒精消毒15s+2%次氯酸钠7min;最佳的启动培养基配方为:MS+6-BA1.0mg/L+NAA0.1mg/L;最佳的增殖培养基配方为:MS+6-BA2.0mg/L+NAA0.5mg/L;最佳的壮苗培养基配方为:1/2MS+I-BA0.1mg/L+NAA0.1mg/L+CCC0.5mg/L。
长筒花(Achimeneserecta)是苦苣苔科长筒花属的多年生草本植物,花腋出,花冠筒状,花径3~8cm,花色有白、粉红、紫、深红、蓝、橘、黄色等[1-2]。目前苦苣苔科植物非洲紫罗兰[3-5]、大岩桐[6-10]等组织培养技术领域的研究已经逐渐趋于完善,而关于长筒花的报道则鲜少见到。本试验通过长筒花叶片离体培养,探究各因素在长筒花的组织培养不同阶段中所产生的作用,并得出各因素的最适水平,进而建立起长筒花的叶片离体培养体系,以利于实现长筒花高品质国产化,以及组培苗的大规模工厂化生产,也为长筒花的分子生物学、细胞学特性研究和基因工程中遗传受体系统的建立奠定理论基础。
长筒花叶片离体培养研究
1材料与方法
1.1材料
试验所用材料为苦苣苔科长筒花属长筒花,品种名为‘kimblue’。
1.2方法
1.2.1筛选最适灭菌组合。
取‘kimblue’叶片,清洗干净后用流水冲洗1h,然后在超净工作台内用不同灭菌组合进行灭菌试验。共设置4个灭菌组合,A1:75%酒精消毒30s,无菌水冲洗2遍,2%次氯酸钠消毒5min,无菌水冲洗4遍;A2:75%酒精消毒30s,无菌水冲洗2遍,2%次氯酸钠消毒7min,无菌水冲洗4遍;A3:75%酒精消毒30s,无菌水冲洗2遍,2%次氯酸钠消毒10min,无菌水冲洗4遍;A4:75%酒精消毒15s,无菌水冲洗2遍,2%次氯酸钠消毒7min,无菌水冲洗4遍。将灭菌完毕的叶片在无菌条件下切成约1cm×1cm方块,接种于培养基中。每个组合接种6瓶,每瓶放置5块叶片,重复3次。1个月后统计叶片的污染率和死亡率。

1.2.2启动培养。
将长筒花‘kimblue’叶片切成1cm×1cm的方块,叶背朝下接入MS培养基,每瓶接种1块叶片。设置不同激素水平(见表1),将6-BA、NAA添加到培养基中[11-12],采取二因素三水平完全随机试验设计,每个处理接30瓶,重复3次。接种45d后统计诱导率,取3次重复平均值记录结果,并记录生长情况,分析不同激素浓度对叶片的启动诱导培养的影响。

1.2.3增殖培养。
将启动诱导培养得到的无菌幼苗用高温灭菌的接种工具(剪刀、镊子、解剖刀)分割成独立单株,或将长高的植株分切成至少带有1个腋芽的节段,接入MS培养基进行增殖扩繁培养,每瓶接入2~3个独立单芽。设置不同6-BA、NAA[13-14]激素水平(表2),采取二因素三水平完全随机试验设计,每个处理接20瓶,重复3次。接种后观察并记录生长状况及增殖情况,30d后统计增殖系数,取3次重复平均值记录结果,分析不同水平激素对叶片的增殖培养的情况。
1.2.4壮苗培养。
不定芽在进行增殖培养后,需要进行壮苗培养才能达到更好的效果。以MS为基本培养基,将生长较好的芽分成单株培养,一些尚未成形的芽分成几个芽丛培养,分别添加不同浓度的6-BA(0mg/L、0.2mg/L、0.5mg/L)、NAA(0.1mg/L、0.3mg/L、0.5mg/L)、IBA(0.1mg/L、0.3mg/L、0.5mg/L)[15-16],采用三因素三水平正交试验设计,每个处理接入20株组培苗,重复3次,比较不同浓度水平的6-BA、NAA、IBA对组培苗壮苗的影响,30d后统计试验结果。筛选出适宜的6-BA、NAA、IBA浓度组合后,进行不同浓度的大量元素母液[15-16]的筛选。设置不同浓度(1/4MS、1/2MS、MS),采用单因素三水平完全随机试验设计,每个处理接入20个组培苗,重复3次,比较不同浓度水平的无机盐对组培苗壮苗的影响,30d后统计试验结果。最后添加不同浓度(0.5mg/L、1.0mg/L、1.5mg/L、2.0mg/L)矮壮素[15,17],采用单因素三水平完全随机试验设计,每个处理接入20株组培苗,重复3次,比较不同浓度水平的矮壮素对组培苗壮苗的影响,30d后统计试验结果。
1.3数据处理
采用Excel和SPSS22软件进行数据统计、方差分析和多重比较,并采用Duncan法进行差异性分析[17]。
2结果与分析
2.1筛选最适灭菌组合
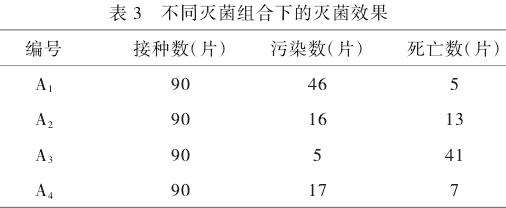
由表3可知,不同的灭菌组合对灭菌效果和活力的影响明显不同。总的来说,叶片的污染率随灭菌时间的延长而下降,死亡率随灭菌时间的延长而上升。从污染片数来看,A2、A3、A4组合污染数较少,从死亡片数上分析来看,A1、A2、A4组合最好,综合2种情况分析来看,A2、A4组合2种灭菌方法处理下的植株污染片数相当,但是A2组合处理下叶片死亡数为13片,多于A4组合的7片。故A4组合对外植体进行灭菌最优。即75%酒精消毒15s后转用无菌水冲洗2遍,再用2%次氯酸钠消毒7min后转用无菌水冲洗4遍。
2.2启动诱导培养
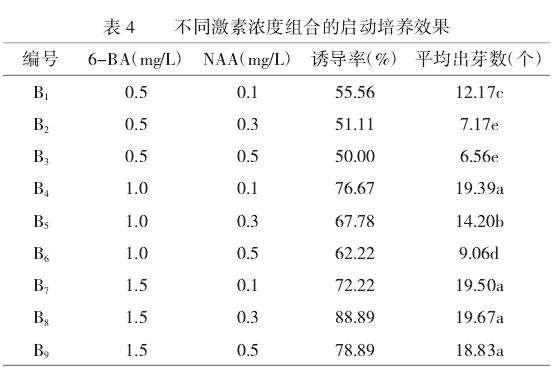
由表4可知,当6-BA浓度分别为0.5mg/L、1.0mg/L、1.5mg/L时,丛生芽平均诱导率在50%、70%、80%水平,即整体上诱导率随着6-BA浓度的增加而上升。在6-BA浓度相同的条件下,诱导率随NAA浓度的增加而有所下降,如B1与B3,B4、B5与B6,B8与B9处理,这可能是由于NAA在一定程度上抑制了6-BA的诱导作用。在诱导率方面,B4、B8和B9的诱导效果显著优于其他配比,分别为76.67%、88.89%和78.89%,其中B8处理诱导率最高,为88.89%,但其叶片玻璃化情况严重,B9处理下叶片也有轻微玻璃化现象,而在B4处理下则生长良好,叶色翠绿。总体来看,B1、B2处理较差,B3、B5和B9生长状况较好,B4生长状况最好,诱导率为76.67%,平均出芽数为19.39。部分处理中出现了玻璃化现象,可能与培养瓶内的湿度、培养基激素浓度有关。
经Duncan法多重比较,6-BA的浓度在启动诱导培养中为主导因素,NAA的浓度起配合辅助作用。
2.3增殖培养
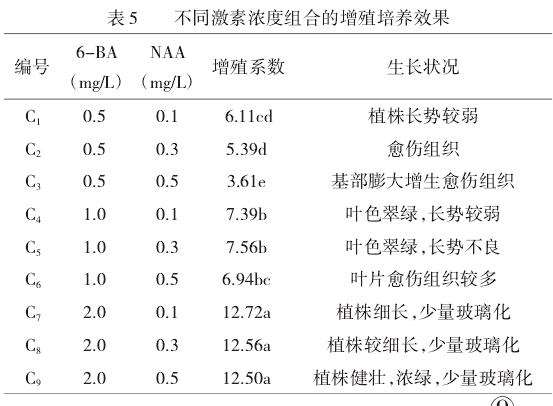
将叶片上诱导产生的不定芽接种于不同浓度的激素配比的增殖培养基上培养。10d左右不定芽开始萌发,15~20d不定芽大量发生。由表5可知,当6-BA浓度为0.5mg/L、1.0mg/L、2.0mg/L时,平均增殖系数分别为5.04、7.30、12.59水平,整体上增殖系数随着6-BA浓度的增加而增加;在6-BA浓度相同的条件下,增殖系数随NAA浓度的增加而有所下降,如C1与C2、C3,C4和C6处理,这可能是由于NAA在一定程度上抑制了6-BA的增殖作用。在增殖方面,C7、C8、C9显著优于其他配比,增殖系数分别为12.72、12.56和12.50,以C7处理的增殖系数最高,但该处理下植株整体呈现细长状态,且有少量玻璃化苗出现;C8处理下植株也呈现细长状态且有少量玻璃化苗;而C9处理下植株虽然也有少量玻璃化苗,但植株整体长势健壮、浓绿。通过观察发现,6-BA浓度相同时,植株健壮程度与NAA浓度成正比,在NAA浓度相同时,增殖系数与6-BA浓度成正比。在C9处理下不定芽增殖数量最多,且生长状况好,植株健壮,叶色浓绿,故C9处理为较合适的激素配比。
经Duncan法多重比较,不同浓度的6-BA、NAA激素组合有显著差异,结果显示6-BA和NAA在增殖培养基中均有重要作用。
2.4壮苗培养
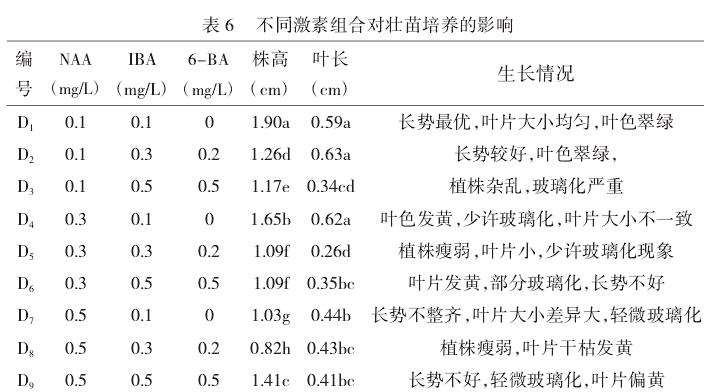
2.4.1不同激素组合对壮苗培养的影响。
由表6可知,当NAA浓度分别为0.1mg/L、0.3mg/L、0.5mg/L时,平均株高分别为1.44cm、1.28cm、1.08cm,平均叶长分别为0.52cm、0.41cm、0.43cm,整体来看,试管苗的株高随着NAA的浓度增加而下降,平均叶长也呈下降趋势。在NAA浓度相同的条件下,长筒花的株高和叶长随着IBA、6-BA浓度增加总体呈下降趋势。如D1与D3,D4与D6,D7与D8处理。通过分析比较,发现D1、D4、D9处理表现最佳,株高、叶长均能达到较高值,D1处理平均株高为1.9cm,平均叶长为0.59cm;D4处理平均株高为1.65cm,平均叶长为0.62cm;D9处理平均株高为1.41cm,平均叶长为0.41cm。分析D1、D4和D7处理发现,影响壮苗效果的主要因素是NAA的浓度,当NAA浓度逐渐增加时,整体长势是呈现下降趋势,当NAA浓度为0.1mg/L时,壮苗效果最佳。从长势来看,长势最佳的是D1、D2处理,整体上呈现较优的状态,叶色翠绿,叶片长势均匀。因此,综合分析,D1处理最适合壮苗培养,植株长势最优,叶片大小均匀,叶色翠绿。
经Duncan法多重比较,6-BA、IBA和NAA在增殖培养基中均有重要作用。
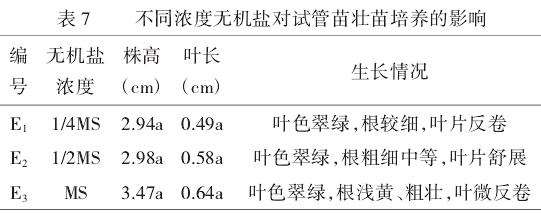
2.4.2不同浓度无机盐对试管壮苗培养的影响。
由表7可知,当无机盐浓度从MS降低到1/2MS时,植株变得健壮,株高变矮;而后随着无机盐浓度降低到1/4MS时,植株株高以及植株的粗壮程度变化不明显。但从整体长势来看,当无机盐浓度为MS浓度时,植株叶色翠绿,根浅黄色、粗壮,叶片微微反卷;当无机盐浓度为1/2MS浓度时,植株叶色翠绿,根粗细中等,叶片舒展;当无机盐浓度为1/4MS浓度时,植株叶色翠绿,根较细,叶片反卷。因此,总体来看,当无机盐浓度为1/2MS时,平均株高为2.98cm,平均叶长为0.58cm,植株总体呈现健壮且叶片舒展的状态,有利于壮苗培养。经方差分析,不同浓度无机盐对壮苗效果没有显著的差异(P>0.05)。
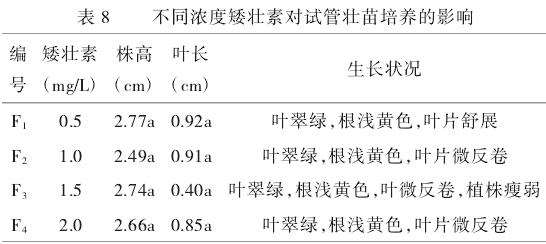
2.4.3不同浓度矮壮素对试管壮苗培养的影响。
由表8可知,F1处理下的幼苗生长情况最佳,植株整体长势良好,叶片舒展,平均株高达2.77cm,平均叶长0.92cm。而在其他处理下时,植株均有不同差异。F2处理的叶片微微反卷,平均株高为2.49cm;F3处理植株长势瘦弱,平均叶长只有0.40cm;F4处理叶片反卷,株高和叶长达到2.66cm和0.85cm。因此,总体来看,当矮壮素浓度为0.5mg/L时,最有利于培养基的壮苗培养。经方差分析,不同浓度矮壮素对壮苗效果无显著差异(P>0.05)。
3结论与讨论
3.1结论
本试验以长筒花的叶片作为外植体,对长筒花叶片进行了完整的启动培养、增殖培养及壮苗培养,研究结果表明,
①综合考虑灭菌后外植体的污染率以及死亡率,长筒花‘kimblue’最适的灭菌组合和方法为:先用75%的酒精消毒15s后用2%次氯酸钠消毒7min。消毒过程中酒精消毒后用无菌水冲洗2遍,次氯酸钠消毒后用无菌水冲洗4次,以免灭菌剂残留造成毒害。
②最佳启动培养的培养基配方为:MS+6-BA1.0mg/L+NAA0.1mg/L,诱导率达76.67%,诱导形成的芽生长状况良好,叶色翠绿。
③增殖培养效果最佳的培养基配方为MS+6-BA2.0mg/L+NAA0.5mg/L,增殖系数为12.5,新增殖的植株健壮,浓绿,仅有少量玻璃化现象。
④壮苗培养基最佳的培养基配方为MS+IBA0.1mg/L+NAA0.1mg/L,平均株高能达到1.9cm,平均叶长0.59cm,植株整体长势最优,叶片大小均匀,叶色翠绿。
⑤壮苗培养基中最佳无机盐浓度为1/2MS,植株平均株高能达到2.98cm,平均叶长0.58cm,整体植株叶色翠绿,根浅黄色,叶片舒展。⑥壮苗培养基中最佳的矮壮素浓度为0.50mg/L,植株平均株高能达到2.77cm,平均叶长0.92cm,植株整体长势良好,叶片舒展,呈翠绿色。
3.2讨论
3.2.1外植体的灭菌处理。
在长筒花‘kimblue’外植体消毒过程中,发现叶片上布满短绒毛,灭菌难度高。试验采用了75%的酒精和2%次氯酸钠作为灭菌试剂,两者均是较为烈性的灭菌试剂,虽然长筒花叶片质地较为粗糙,承受强度较大,但仍有承受限度,因此在消毒时间上应严格把控,时间过短无法起到灭菌作用,也会造成大量污染,时间过长则易对外植体组织造成不可逆的损伤,且死亡率高。
3.2.2激素在长筒花组织培养中的作用。
一般植物组培苗的培养途径有不定芽、愈伤组织、器官发生、原球茎等[18-25],大部分研究是通过外植体[26-27]直接诱导出不定芽,可大大减少再生体系的建立时间,因此本试验中选用了叶片作为长筒花试验的外植体,直接诱导不定芽,再通过不定芽增殖及生根,建立长筒花立体叶片的离体培养体系[28]。
在启动诱导阶段和增殖培养中,常用的激素种类主要有6-BA和NAA,其中6-BA在不定芽的诱导中必不可少,在试验中与NAA搭配使用。本试验结果表明,在启动培养阶段,合理范围内较高浓度的6-BA效果较好,且6-BA和NAA的比例不能过小;在增殖培养阶段,较高浓度的NAA有利于不定芽的健壮生长,但抑制增殖数量,故适宜的6-BA和NAA的浓度配比对长筒花不定芽的增殖和诱导非常重要。在壮苗培养阶段,降低无机盐浓度和矮壮素浓度可以使植株生长更健壮。鉴于不同种或品种的长筒花由于生物学形状上的差异,对适宜的激素组合存在差异,在进行大批量生产前,应进行针对性研究,得出最适宜、最有效的激素种类和配比,再应用于生产之中。